冷冻保存是 细胞和基因治疗 研究,使 长期储存 以及 运输 生物材料,同时力求保持其活力和功能。对于敏感细胞类型——例如 间充质干细胞(MSCs) 、CAR-T 细胞和诱导性多能干细胞 (iPSC)——这个过程风险特别高,其中冷冻介质的每个成分都可能决定治疗的成功或失败。
为了减轻冰晶形成的破坏作用,冷冻保护剂如 二甲基亚砜(DMSO) 以及 蛋白质, 通常以胎牛血清(FBS)或人血清白蛋白(HSA)的形式使用。然而,如果不谨慎管理,这些添加剂会带来重大风险,尤其是对于用于临床应用的细胞而言。
在本篇博文中,我们探讨了冻存介质中DMSO和蛋白质的隐患——从细胞毒性、批次差异到免疫原性问题——以及研究人员为何必须谨慎处理这些成分。透彻了解这些风险对于制定优化的冻存策略至关重要,从而确保细胞和基因疗法的可靠性、安全性和治疗潜力。
细胞和基因治疗中的当前冷冻保存策略 细胞和基因治疗的成功取决于在不损害细胞产品活力、功能或治疗潜力的情况下保存细胞产品的能力。 冷冻保存 将细胞冷却至超低温(通常使用液氮约为-80°C或-196°C)的过程可以停止细胞的代谢活动,从而实现长期储存和运输。然而,冻融过程本身也带来了重大挑战,包括 冰晶形成 , 渗透压 和 氧化损伤 ,所有这些都会损害细胞的存活和性能。
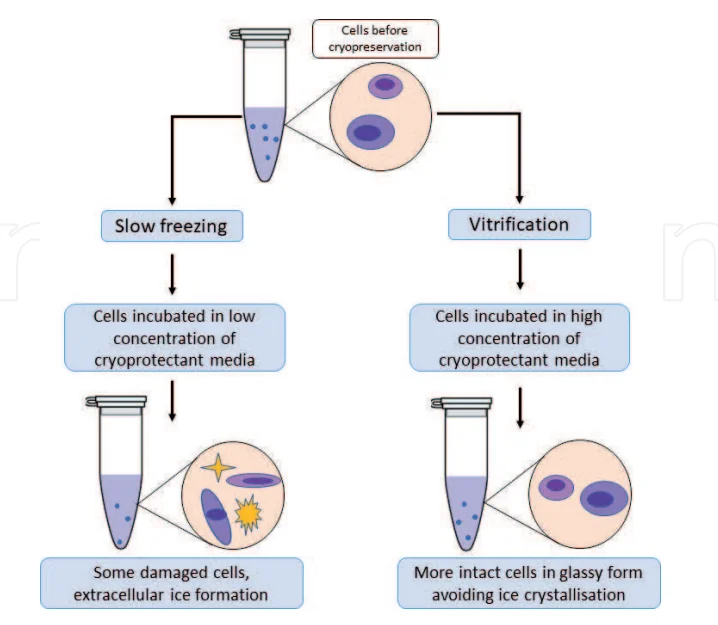
为了降低这些风险,优化的冷冻保存方案必须平衡冷却速率、储存条件和使用 冷冻保护剂(CPA)。 通常采用两种主要方法:
一种广泛使用的方法,将细胞冷却至 控制速率约为每分钟 −1°C .这个速率允许 水离开细胞质 ,然后部分被 CPA(如 DMSO)取代。目的是 尽量减少细胞内冰的形成 ,这会导致膜破裂和活力丧失。 细胞膜通透性 确保在冰晶形成之前有足够的时间进行水分流出和CPA吸收。慢速冷冻通常使用 控温冷冻机 or 冷冻容器 .低污染风险 其特点是无需手动操作,且广泛适用于各种细胞类型,包括用于细胞和基因治疗研究的细胞。此外,它还能提供一致的结果,无需专业的冷冻保存专业知识。
An 超快速冷却技术 将水性细胞悬浮液直接暴露于液氮中,使溶液立即转变为 玻璃状、无冰状态 这种方法避免了冰晶的形成,从而避免了破坏细胞结构,使得玻璃化冷冻特别有效 高度敏感的细胞 如 卵母细胞和某些干细胞 .高浓度的注册会计师 -通常 40–60%(重量/体积) —防止冰核形成。为了成功,玻璃化需要 极快的冷却和升温速度 ,同时仔细控制变量,例如 取样量 , 粘性 ,并 CPA 混合物的精确配方 .最大程度减少冻害的主要优势 和保存 解冻后活力高 ,它带来了一些挑战。其中包括 CPA毒性 精确的操作技巧 不可忽视的微生物污染风险
尽管取得了这些进展,CPA 的选择仍然是一个关键变量。蛋白质(例如血清白蛋白)和 DMSO 等小分子添加剂被广泛使用,但在安全性、一致性和解冻后恢复方面存在诸多缺点。以下章节将探讨这些关键成分在细胞和基因治疗应用中的优势、局限性和风险。
DMSO 在冷冻保存中的作用:平衡功效与毒性 自推出以来的60年里,DMSO一直是冷冻保存的基石,彻底改变了活细胞的长期储存方式。作为最 广泛使用的穿透CPA ,它对于保存敏感细胞类型至关重要。然而,尽管DMSO有效,它也带来了从细胞毒性到临床副作用等诸多挑战,促使研究人员寻求更安全的替代品。
为什么 DMSO 是冷冻保存的黄金标准 DMSO 长期以来一直被认为是黄金标准 CPA,因为它 独特的穿透细胞膜的能力 以及 防止细胞内冰形成 ,这是冷冻过程中细胞受损的主要原因。
其占据主导地位的关键原因:
膜渗透性 :DMSO 能快速进入细胞并与细胞内环境达到平衡。通过减少可冻水的含量,防止细胞内形成冰晶。低浓度下有效 :通常用于 5–10%(体积比) ,DMSO 提供了出色的保护,而不需要过高的浓度来增加毒性。广泛的适用性 :DMSO 与 多种细胞类型 —包括造血干细胞、MSCs、淋巴细胞和各种原代和永生化细胞系——使其成为研究和临床应用的多功能工具。临床验证 : DMSO 在 临床冷冻保存方案 包括造血干细胞移植。其疗效和安全性已在监管框架中得到充分证实。成本效益和可用性 :它广泛可用、在室温下稳定且经济实惠,使其成为研究实验室和商业生物库的实用选择。
DMSO 的主要局限性和风险
尽管 DMSO 在研究和临床冷冻保存中得到广泛应用,但它也存在一些重大风险。其细胞毒性、损害细胞功能的可能性以及临床副作用,引发了人们对其长期适用性的严重担忧,尤其是在 细胞和基因治疗应用 其中产品完整性和患者安全至关重要。
1. 细胞毒性和功能障碍
虽然 DMSO 可以有效防止细胞内冰的形成,但它本质上 对细胞有毒 对于某些敏感细胞类型,即使浓度低至 5–10%。
细胞代谢紊乱 :DMSO 可能会损害 线粒体呼吸 ,诱导 氧化应激 和损害 细胞膜 。这些影响在解冻阶段尤为明显,因为此时细胞最脆弱。解冻后活力和功能的丧失 :某些免疫细胞——例如 自然杀伤细胞 , 树突细胞 和 CAR-T细胞 —对DMSO暴露高度敏感。解冻后,这些细胞可能表现出 可行性 , 增殖能力 和 效应功能 ,限制了它们的治疗效用。表观遗传和转录扰动 :长期接触 DMSO 可能导致 基因表达的变化 以及 表观遗传修饰 ,这可能会损害 效力、身份和稳定性 治疗细胞产品。这些影响可能会给生产带来变化,并引发对法规遵从性的担忧。
2. 患者的临床副作用
输注含有 DMSO 的细胞产品可能会导致 患者不良反应 ,特别是涉及大量或高浓度时。
急性输液相关反应 :常见的副作用包括 恶心、呕吐、腹部绞痛、低血压或高血压 ,并且在某些情况下, 类似过敏反应 心血管和神经系统事件 :在罕见但严重的情况下,DMSO 输注与 心动过缓、癫痫和脑病 —尤其是儿童或免疫功能低下的患者溶血风险 :残留的 DMSO 可能导致 红细胞膜不稳定性 如果输注中含有红细胞成分或解冻后未彻底清洗,则可能导致溶血
3. 监管和制造挑战
DMSO 带来了一些挑战,使细胞疗法的扩大和临床转化变得复杂:
临床级 DMSO 要求: 当用于细胞治疗生产时,DMSO 必须满足 严格的质量标准 (例如,USP 或 Ph. Eur. 级),并且其处理需要仔细记录以满足良好生产规范 (GMP) 环境的监管要求。供应商之间的不一致: 不同制造商的 DMSO 纯度和性能可能存在差异,这可能会影响冷冻保存方案的可重复性。在扩大监管备案或临床级生产规模时,这种不一致性至关重要。下游加工负担: 解冻后去除残留的DMSO(通常通过稀释或清洗)会增加时间和复杂性。这些步骤可能导致细胞大量丢失、功能改变或活化诱导的细胞凋亡,最终导致 降低产量和产品一致性 .DMSO 最小化的行业趋势: 虽然没有强制要求,但许多开发人员积极主动 降低 DMSO 浓度 或探索 不含 DMSO 的替代品 以满足人们对更安全、更明确的细胞治疗产品不断变化的期望。
为什么蛋白质需要冷冻保存 蛋白质——特别是血清衍生的蛋白质,如 白蛋白 以及 FBS —在传统的冷冻保存方案中发挥着多种关键作用。它们的加入有助于减轻冻融过程中机械、渗透和氧化应激对细胞造成的损伤。
1. 膜稳定和冰重结晶抑制 在冷冻保存过程中,细胞容易受到 冰晶引起的机械损伤 尤其是在解冻过程中,重结晶可能会加剧损伤。蛋白质可以通过以下几种方式提供帮助:
表面保护 :蛋白质如 白蛋白 吸附到细胞膜上,形成 水合保护层 最大限度地减少与冰晶的直接接触。这种缓冲作用可以减少膜破裂和机械应力冰重结晶抑制 :一些蛋白质模仿自然界中发现的抗冻蛋白的作用,有助于 调节冰晶生长 以及 抑制再结晶 这对于保存干细胞和免疫细胞等脆弱的细胞类型至关重要。胶体稳定性 :白蛋白和其他蛋白质起着 胶体稳定剂 ,防止 细胞聚集 冷冻和解冻阶段均能有效防止细胞聚集。这可以提高细胞悬浮液的均匀性,并简化下游加工。
2. 缓解渗透和氧化胁迫 冻融循环对 渗透压变化和氧化应激 ,这两者都会损害细胞活力。
渗透保护 :蛋白质有帮助 缓冲渗透失衡 通过调节跨膜的水运动和溶质浓度。这减少了 细胞过度收缩或肿胀 否则会造成不可逆的膜损伤。抗氧化能力 :血清类冷冻保存剂(如 FBS)天然含有 抗氧化剂 ,包括 谷胱甘肽和过氧化氢酶 ,有助于中和 活性氧 (ROS) 解冻过程中产生的抗氧化剂缓冲剂可以限制细胞成分的氧化损伤,并防止 细胞凋亡级联 由压力引发。
3. 生长因子和解冻后恢复支持 除了在冷冻保存期间提供直接保护外,蛋白质还有助于 解冻后恢复 ,特别是对于敏感或代谢活跃的细胞:
生物活性 :FBS 富含 生长因子、激素、细胞因子、脂质和维生素 . 这些分子支持细胞 代谢、增殖和修复 解冻后的机制。干细胞支持 : 如果是 间充质干细胞 、造血干细胞(HSC)和原代细胞,FBS 中的复杂环境可以增强 恢复和重新附着 ,加速恢复正常功能。
蛋白质添加剂——并非总是无害的 虽然蛋白质 FBS , HSA 或 血浆衍生物 因其保护作用而被广泛应用于冷冻保存,它们具有 重大风险 —尤其是在开发时 临床级或可重复的研究产品 。这些风险在以下情况下尤其令人担忧: 细胞和基因治疗 其中产品的一致性、纯度和安全性至关重要。
1. 批次间差异 生物衍生蛋白质(尤其是 FBS)最紧迫的问题之一是 批次间差异 即使来自同一供应商,不同批次的产品在蛋白质含量、渗透压或存在不明因素方面也可能存在差异。这种差异可能导致:
不可预测的冷冻保存结果 ,包括不一致的细胞活力和恢复。困难中 扩大 或将协议从研究转移到 GMP 设置。
面临的挑战 工艺验证 ,这是获得监管部门批准的关键一步。
2. 免疫原性和污染风险 来自动物或混合人类血浆的蛋白质可能会引入不必要的 异种抗原或同种抗原 ,这可以触发 免疫反应 在患者中——特别是在同种异体细胞疗法中。
此外,这些蛋白质补充剂还存在以下风险 生物污染物 多种大口径枪械:
内毒素 这可能会引发细胞因子风暴。朊病毒 或逃避过滤的病毒颗粒。未知的外来因素 这在监管检查中引起了警觉。
即使是“临床级”人血白蛋白也并非完全没有风险。这些污染物的存在使得 GMP生产 以及 监管许可 用于临床应用。
3. 对下游应用的干扰 除了安全问题外,蛋白质添加剂还可能 使下游流程复杂化 特别是在 基因治疗和EV研究 :
中 转导 or 电穿孔 ,蛋白质可以 抑制病毒进入 ,降低转染效率,或促进聚集。
In 细胞外囊泡(EV) 研究表明,血清来源的蛋白质可能 污染电动汽车制剂 ,导致假阳性结果或受损的生物标志物分析。
In 蛋白质组学或组学工作流程 ,残留蛋白质可能会引入 背景噪音 ,掩盖关键信号或引入伪影。
迈向定义,Xeno - 免费 备择方案 上述安全、监管和供应链压力加速了从 “经典”FBS + 10%DMSO 食谱 化学 - 已定义,异种 - 免费冷冻保存 系统。许多商业制造商已经开发出下一代培养基,用重组或合成的稳定剂取代血清和其他动物源性成分,并且在许多情况下显著减少或完全消除了 DMSO。
比较喜欢 0% 二甲基亚砜 用于自体输注或非常敏感的细胞(例如 MSCs、iPSCs、NK 细胞)。
对于某些 DMSO 仍然有利的产品,上限为 ≤ 5% 并规划快速、封闭系统清洗步骤。
运行试点冻融研究,测量活力、表型(流式细胞术)、效力/读数(例如 MSCs 的 CFU-F、CAR-T 的细胞毒性)。
确认 实用 恢复,而不仅仅是膜的完整性。
保持~1 °C · min⁻¹ 冷却(慢速冷冻),除非产品需要玻璃化。
采用封闭的袋子或小瓶形式,以避免微生物进入并保留 GMP 身份链。
快速升温(30°C 水浴 60-37 秒),在 ≤10分钟 并在 BSC 中完成清洗,以尽量减少细胞毒性作用——即使使用“低毒”CPA。
CryoEase-PF:更安全、更精准的敏感细胞保存方案 CryoEase-PF 化学成分明确的无外来物质溶液 专为保存和运输敏感细胞(包括 MSCs)而配制。
主要优势:
不含 DMSO 和蛋白质的成分: 通过消除 DMSO 和动物源性蛋白质,CryoEase-PF 降低了细胞毒性和变异性,确保了更高的解冻后细胞活力和功能完整性。双温度兼容性: CryoEase-PF 在零下(-80°C)和低温(4-10°C)下均有效,为各种储存和运输条件提供了灵活性。增强细胞活力: 研究表明,使用 CryoEase-PF 保存的 MSCs 在 85°C 下保存 72 小时后仍可保持 4% 以上的活力,优于在类似条件下活力低于 75% 的其他配方。保持功能完整性: 解冻后,MSCs 表现出一致的群体倍增时间并保留其三系分化潜力,符合国际细胞和基因治疗学会 (ISCT) 设定的标准。符合 GMP 标准的材料: CryoEase-PF 采用符合 GMP 标准的材料制成,支持从研究到临床应用的无缝过渡,甚至跨越国界。
CryoEase-PF 的创新配方 简化物流 通过减少对复杂 冷链系统 使其成为敏感电池在国内和国际运输的理想选择。它兼容 短期低温储存 以及 长期冷冻保存 为研究人员和临床医生提供了一种在运输和储存过程中保持细胞质量的多功能解决方案。
参考文献:
Aljaser, Feda. 冷冻保存方法及动物模型冷冻生命技术前沿。2022 10.5772/intechopen.101750。DOI:10.5772/intechopen.101750
Amini M,Benson JD。基于玻璃化冷冻保存的技术。《生物工程》(巴塞尔)。2023年23月10日;5(508):10.3390。doi: 10050508/bioengineeringXNUMX。
Awan M, Buriak I, Fleck R, Fuller B, Goltsev A, Kerby J, Lowdell M, Mericka P, Petrenko A, Petrenko Y, Rogulska O, Stolzing A, Stacey GN. 二甲基亚砜:自低温生物学诞生以来的核心作用,其疗效是否与毒性相平衡?《再生医学》(Regen Med)2020年15月;3(1463):1491-10.2217. doi: 2019/rme-0145-2020. 电子版发布于28年XNUMX月XNUMX日。
Ekpo MD, Boafo GF, Xie J, Liu X, Chen C, Tan S. 生物治疗药物无二甲基亚砜 (DMSO) 冷冻保存方案的开发策略。Front Immunol. 2022年5月13日;1030965:10.3389. doi: 2022.1030965/fimmu.XNUMX.
Erol OD, Pervin B, Seker ME, Aerts-Kaya F. 储存介质、补充剂及冻存方法对干细胞质量的影响。《世界干细胞杂志》。2021年26月13日;9(1197):1214-10.4252. doi: 13/wjsc.v9.1197.iXNUMX。
Fujita Y, Nishimura M, Komori N, Sawamoto O, Kaneda S. 含海藻糖和葡聚糖40的无蛋白溶液用于冷冻保存人脂肪组织来源的间充质基质细胞。《低温生物学》。2021年100月;46:57-10.1016。doi: 2021.03.011/j.cryobiol.2021。电子版发布日期:3年XNUMX月XNUMX日。
Jaiswal AN、Vagga A. 冷冻保存:评论文章。库鲁乌斯。 2022 年 16 月 14 日;11(31564):e10.7759。 doi:31564/cureus.XNUMX。
Joules A, Mallya AS, Louwagie T, Yu G, Hubel A. 探索冷冻保存对自然杀伤细胞的损伤机制。《细胞治疗》。2025年25月1465日:S3249-25(00035)0-10.1016。doi: 2025.01.012/j.jcyt.XNUMX。
Weng L. 细胞治疗药物产品开发:技术考量与挑战。《药物科学杂志》,2023年112月;10(2615):2620-10.1016。doi: 2023.08.001/j.xphs.2023。电子版发布日期:6年XNUMX月XNUMX日。
Whaley D, Damyar K, Witek RP, Mendoza A, Alexander M, Lakey JR. 冷冻保存:原理及细胞特异性注意事项概述。《细胞移植》。2021年30月-963689721999617月;10.1177:0963689721999617。doi: XNUMX/XNUMX。
Windrum P, Morris TC, Drake MB, Niederwieser D, Ruutu T; EBMT 慢性白血病工作组并发症小组委员会。二甲基亚砜在干细胞移植中的应用差异:EBMT 中心调查。《骨髓移植》。2005年36月;7(601):3-10.1038。doi: 1705100/sj.bmt.16044141。PMID: XNUMX。